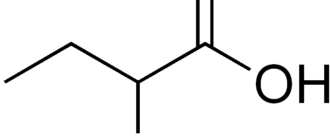
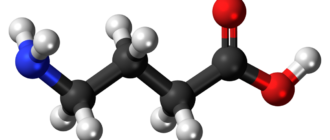
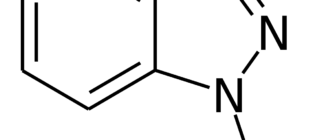
Цистин (3, 3′-дитио-бис-2-аминопропионовая к-та, дицистеин) — алифатическая серосодержащая аминокислота, бесцветные кристаллы, плохо растворимы в холодной воде, растворимы в минеральных кислотах и органических растворителях.
| Цистин | |
|---|---|
| Общие | |
| Хим. формула | C6H12N2O4S2 |
| Рац. формула | C6H12N2O4S2 |
| Физические свойства | |
| Молярная масса | 240.24 г/моль |
| Классификация | |
| Рег. номер CAS | 56-89-3 |
| PubChem | 67678 |
| Рег. номер EINECS | 200-296-3 |
| SMILES |
C(C(C(=O)O)N)SSCC(C(=O)O)N
|
| InChI |
1S/C6H12N2O4S2/c7-3(5(9)10)1-13-14-2-4(8)6(11)12/h3-4H,1-2,7-8H2,(H,9,10)(H,11,12)/t3-,4-/m0/s1
LEVWYRKDKASIDU-IMJSIDKUSA-N
|
| ChEBI | 16283 и 35491 |
| ChemSpider | 60997 |
Цистин — некодируемая аминокислота, представляющая собой продукт окислительной димеризации цистеина, в ходе которой две тиольные группы цистеина образуют дисульфидную связь цистина. Цистин содержит две аминогруппы и две карбоксильных группы и относится к двухосновным диаминокислотам.
В организме находятся в основном в составе белков.
Биологическая роль

Структура окситоцина: пентапептидный цикл замыкается внутримолекулярным дисульфидным мостиком
Дисульфидные цистиновые мостики, образуемые цистеиновыми остатками в ходе посттрансляционной модификации белков, играют крайне важную роль в формировании и поддержании третичной структуры белков и пептидов и, соответственно, их биологической активности. Так, например, такие гормоны, как вазопрессин, окситоцин и соматостатин приобретают биологическую активность после образования внутримолекулярных дисульфидных мостиков, инсулин представляет собой две пептидные цепи, соединенные дисульфидными мостиками.
Образование многочисленных остатков цистина, соединяющих дисульфидными связями пептидные цепи в кератинах, обуславливает их высокую жесткость, так, в кератине волос содержание цистина (с цистеином) составляет ~18%.
Производство и применение
Производят окислением тиольных групп цистеина в щелочных растворах(щелочь-катализатор). Является частью лекарственных препаратов. Мировое производство — десятки тонн в год.