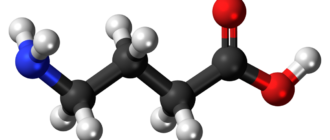
Трис — сокращённое название химического соединения трис(гидроксиметил)аминометана3CNH2. Трис широко используется в биохимии и молекулярной биологии в качестве буферного раствора, например, в буферных системах TAE и TBE, для растворения нуклеиновых кислот. По химической структуре трис является первичным амином и имеет характерные для аминов свойства, например, конденсируется с альдегидами.
| Трис | |
|---|---|
| Общие | |
| Систематическое наименование |
2-амино-2-гидроксиметил-пропан-1,3-диол |
| Сокращения | THAM |
| Традиционные названия | ТРИС, трис, Trizma™ |
| Хим. формула | C4H11NO3 |
| Физические свойства | |
| Молярная масса | 121,14 г/моль |
| Термические свойства | Температура |
| • плавления | 175—176 °C |
| • кипения | 219 °C |
| Химические свойства | Растворимость |
| • в воде | ~50 г/100 мл |
| Классификация | |
| Рег. номер CAS | 77-86-1 |
| PubChem | 6503 |
| Рег. номер EINECS | 201-064-4 |
| SMILES |
OCC(N)(CO)CO
|
| InChI |
1S/C4H11NO3/c5-4(1-6,2-7)3-8/h6-8H,1-3,5H2
LENZDBCJOHFCAS-UHFFFAOYSA-N
|
| RTECS | TY2900000 |
| ChEBI | 9754 |
| ChemSpider | 6257 |
| Безопасность | |
| NFPA 704 |
|
Буферные свойства
Трис имеет pKa 8,06, и эффективен в качестве буфера при pH от 7,0 до 9,2.
Значение pKa снижается приблизительно на 0,03 при снижении температуры на один градус Цельсия.
Широко распространённый вариант буферного раствора, Трис-HCl, является кислой солью. Когда pH раствора соответствует pKa, концентрации противоионов равны (OH- для трис-HCl и H+ для трис-основания).
Показано, что трис ингибирует некоторые ферменты, и поэтому при изучении белков должен использоваться с осторожностью.
Синтез
Трис синтезируют в две стадии из нитрометана через интермедиат (HOCH2)3CNO2. Восстановление последнего дает трис(гидроксиметил)аминометан.
Применение
Буферные свойства при рН 7—9 соответствуют физиологическим значениям рН для большинства организмов. Эти свойства и низкая стоимость делают трис одним из лучших буферов для биохимии и молекулярной биологии. Трис используют в качестве первичного стандарта для растворов кислот при химическом анализе.
Трис используют в качестве альтернативы гидрокарбонату натрия при лечении метаболического ацидоза.