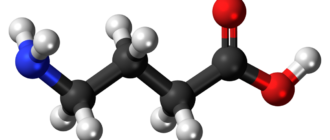
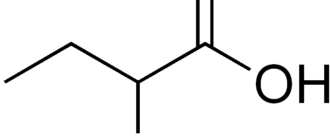
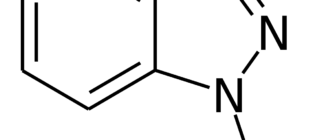
Тирозинпропионовая кислота, сокр.: Тир, Tyr, Y) — ароматическая альфа-аминокислота. Существует в двух оптически изомерных формах — L и D и в виде рацемата. По строению соединение отличается от фенилаланина наличием фенольной гидроксильной группы в пара-положении бензольного кольца. Известны менее важные с биологической точки зрения мета- и орто- изомеры тирозина.
| Тирозин | |
|---|---|
| Общие | |
| Систематическое наименование |
2-амино-3-(4- гидроксифенил) пропановая кислота |
| Сокращения | Тир, Tyr, Y UAU,UAC |
| Хим. формула | C9H11NO3 |
| Рац. формула | C9H11NO3 |
| Физические свойства | |
| Молярная масса | 181,19 г/моль |
| Плотность | 1,456 г/см³ |
| Термические свойства | Температура |
| • плавления | 343 °C |
| Химические свойства | |
| Константа диссоциации кислоты | 2,24 9,04 10,10 |
| Изоэлектрическая точка | 5,66 |
| Классификация | |
| Рег. номер CAS | [60-18-4] |
| PubChem | 6057 |
| Рег. номер EINECS | 200—460-4 |
| SMILES |
C1=CC(=CC=C1CC(C(=O)O)N)O
|
| InChI |
1S/C9H11NO3/c10-8(9(12)13)5-6-1-3-7(11)4-2-6/h1-4,8,11H,5,10H2,(H,12,13)/t8-/m0/s1
OUYCCCASQSFEME-QMMMGPOBSA-N
|
| ChEBI | 17895 и 58315 |
| ChemSpider | 5833 |
| Безопасность | |
| NFPA 704 |
|
L-тирозин является протеиногенной аминокислотой и входит в состав белков всех известных живых организмов. Тирозин входит в состав ферментов, во многих из которых именно тирозину отведена ключевая роль в ферментативной активности и её регуляции. Местом атаки фосфорилирующих ферментов протеинкиназ часто является именно фенольный гидроксил остатков тирозина. Остаток тирозина в составе белков может подвергаться и другим посттрансляционным модификациям. В некоторых белках (резилин насекомых) присутствуют молекулярные сшивки, возникающие в результате посттрансляционной окислительной конденсации остатков тирозина с образованием дитирозина и тритирозина.
Окрашивание в результате ксантопротеиновой качественной реакции на белки определяется преимущественно нитрованием остатков тирозина (нитруются также остатки фенилаланина, триптофана, и гистидина).
Биосинтез
В процессе биосинтеза тирозина промежуточными соединениями являются шикимат, хоризмат, префенат. Из центральных метаболитов тирозин в природе синтезируют микроорганизмы, грибы и растения. Животные не синтезируют тирозин de novo, но способны гидроксилировать незаменимую аминокислоту фенилаланин в тирозин. Более подробно биосинтез тирозина рассмотрен в статье шикиматный путь.
Тирозин относят к заменимым для большинства животных и человека аминокислотам, так как в организме эта аминокислота образуется из другой (незаменимой) аминокислоты — фенилаланина.
Катаболизм
В организм животных и человека тирозин поступает с пищей. Также тирозин образуется из фенилаланина (реакция протекает в печени под действием фермента фенилаланин-4-гидроксилазы). Превращение фенилаланина в тирозин в организме в большей степени необходимо для удаления избытка фенилаланина, а не для восстановления запасов тирозина, так как тирозин обычно в достаточном количестве поступает с белками пищи, и его дефицита, как правило, не возникает. Избыток тирозина утилизируется. Тирозин путём переаминирования с α-кетоглутаровой кислотой превращается в 4-гидроксифенилпируват, который далее окисляется (с одновременной миграцией и декарбоксилированием кетокарбоксиэтильного заместителя) в гомогентизат. Гомогентизат через стадии образования 4-малеилацетоацетата и 4-фумарилацетоацетата распадается до фумарата и ацетоацетата. Окончательное разрушение происходит в цикле Кребса.
Таким образом, у животных и человека тирозин распадаются до фумарата (превращается в оксалоацетат, являющийся субстратом глюконеогенеза) и ацетоацетата (повышает уровень кетоновых тел в крови), поэтому тирозин, а также превращающийся в него фенилаланин, по характеру катаболизма у животных относят к глюко-кетогенным (смешанным) аминокислотам .
В природе известны и другие пути биодеградации тирозина.
Из тирозина синтезируются такие биологически активные вещества, как ДОФА, тиреоидных гормонов (тироксин, трийодтиронин). ДОФА является предшественником катехоламинов (дофамин, адреналин, норадреналин) и пигмента меланина. Гомогентизат является предшественником токоферолов, пластохинона (у организмов, способных синтезировать эти соединения).
С обменом тирозина связаны некоторые известные наследственные заболевания. При наследственном заболевании фенилкетонурии превращение фенилаланина в тирозин нарушено, и в организме происходит накопление фенилаланина и его метаболитов (фенилпируват, фениллактат, фенилацетат, орто-гидроксифенилацетат, фенилацетилглутамин), избыточное количество которых отрицательно сказывается на развитии нервной системы. При другом известном наследственном заболевании — алкаптонурии — нарушено превращение гомогентизата в 4-малеилацетоацетат.
Известно также несколько относительно редких заболеваний (тирозинемии), вызванных нарушениями обмена тирозина. Лечение этих заболеваний, как и фенилкетонурии — диетическое ограничение белка.
Применение
Тирозин подавляет аппетит, способствует уменьшению отложения жиров, способствует выработке меланина и улучшает функции надпочечников, щитовидной железы и гипофиза.