Морфолин — гетероциклическое соединение. Химическая формула HN(CH2CH2)2O.
| Морфолин | |
|---|---|
| Общие | |
| Систематическое наименование |
тетрагидрооксазин-1,4 |
| Традиционные названия | морфолин |
| Хим. формула | C4H9NO |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 87,1 г/моль |
| Плотность | 1,007 г/см³ |
| Энергия ионизации | 8,88 ± 0,01 эВ |
| Термические свойства | Температура |
| • плавления | -5 °C |
| • кипения | 129 °C |
| • вспышки | 98 ± 1 °F |
| Пределы взрываемости | 1,4 ± 0,1 об.% |
| Давление пара | 6 ± 1 мм рт.ст. |
| Химические свойства | |
| Константа диссоциации кислоты | 8,33 | Растворимость |
| • в воде | смешивается |
| Оптические свойства | |
| Показатель преломления | 1,4545 |
| Структура | |
| Дипольный момент | 1,58 Д |
| Классификация | |
| Рег. номер CAS | 110-91-8 |
| PubChem | 8083 |
| Рег. номер EINECS | 203-815-1 |
| SMILES |
O(CCNC1)C1
|
| InChI |
1S/C4H9NO/c1-3-6-4-2-5-1/h5H,1-4H2
YNAVUWVOSKDBBP-UHFFFAOYSA-N
|
| RTECS | QD6475000 |
| ChEBI | 34856 |
| ChemSpider | 13837537 |
| Безопасность | |
| Предельная концентрация | 0,5 мг/м³ |
| ЛД50 | 15-100 мг/кг |
| Токсичность | Класс опасности 2 |
| NFPA 704 |
|
Ядовит.
Используется в органическом синтезе как катализатор в качестве основания (акцептор протона), в частности, для получения геминальных дитиолов.
История
Морфолин впервые синтезировал в 1889 году немецкий химик-органик Людвиг Кнорр и он же дал веществу название, ошибочно полагая, что эта структурная единица входит в молекулу морфина.
Физические свойства
Бесцветная гигроскопичная жидкость со слабым аминным запахом рыбы.
Смешивается с водой, ацетоном, диэтиловым эфиром.
Молекула морфолина имеет конформацию в виде «кресла».
Химические свойства
Морфолин вступает в большинство реакций, характерных для вторичных аминов. Благодаря атому кислорода, оттягивающего электронную плотность на себя от атома азота, он менее нуклеофильный и менее основный, чем структурно аналогичный вторичный амин, такой как, например, пиперидин. Поэтому он образует стойкий хлорамин.
Получение
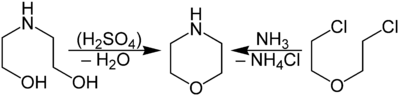
Морфолин получают дегидратацией диэтаноламина или аминированием бис(2-хлорэтилового)эфира.
Схема синтеза морфолина:
Очистка
Для очистки его сушат над сернокислым кальцием, после чего с осторожностью дробно перегоняют. Рекомендуют также перегонку или высушивание над металлическим натрием, либо высушивание над гидроксидом калия (KOH), перегонкой, выдерживанием над металлическим натрием и повторной перегонкой.
Применение
В промышленности
Морфолин — ингибитор коррозии. Морфолин — обычная добавка с концентрацией в миллионных долях, для регулирования pH как в топливных системах с использованием минеральных топлив, так и в системах охлаждения ядерных реакторов. С этой целью морфолин применяется из-за его летучести близкой к летучести воды, то есть, при добавлении морфолина в воду, его концентрации в воде и парах примерно одинаковы и он распространяется вместе с водяным паром через весь парогенератор, обеспечивая регулирование pH и защиту от коррозии.
Морфолин достаточно устойчив и медленно разлагается в отсутствие кислорода при высоких температурах и давлениях в парогенераторах.
Используется в качестве абсорбента для очистки газов от CS2 и карбонилсульфида (COS).
Органический синтез
Морфолин широко используется в органическом синтезе. Например, он входит в антибиотик линезолида и противораковый препарат Gefitinib.
Он также широко используется для получения енаминов.
Морфолин используется в качестве амина в модификации Киндлера реакции Вильгеродта для получения ω-арилалкановых кислот.
В исследованиях и в промышленности, дешевизна и полярные свойства морфолина привела к его широкому применению в качестве растворителя для реагентов химических реакций.
Безопасность
Морфолин — легковоспламеняющаяся жидкость. Температура вспышки 35 °С, температура самовоспламенения 230 °С. Пары раздражают слизистые оболочки дыхательных путей, при попадании на кожу вызывают жжение. ЛД50 15-100 мг/кг (мыши и морские свинки, перорально); ПДК 0,5 мг/м3.