Адренокортикотропный гормон, или АКТГ, кортикотропин, адренокортикотропин, кортикотропный гормон — тропный гормон, вырабатываемый базофильными клетками передней доли гипофиза. По химическому строению АКТГ является пептидным гормоном.
| Производные проопиомеланокортина: | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Проопиомеланокортин | |||||||||
| γ-MSH | АКТГ | β-липотропин | |||||||
| α-MSH | CLIP | γ-липотропин | β-эндорфин | ||||||
| β-MSH | |||||||||
Строение
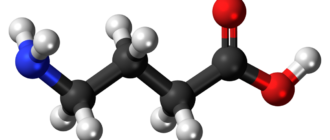
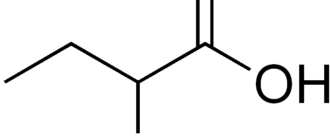
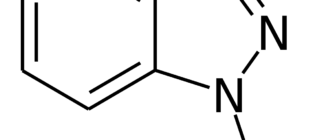
Молекула АКТГ человека состоит из 39 аминокислотных остатков (4,540 Да). Характеристики АКТГ определяются различными участками его пептидной цепи: участок с 4 по 10 аминокислоту является актоном (пептидом, определящим функцию, синтетический аналог этого участка — препарат Семакс), с 15 по 21 (особенно с 15 по 18) аминокислоту — гаптоном (пептидом, определяющим специфичность связывания с рецептором). Участок с 1 по 3 и с 11 по 13, по-видимому, обуславливает меланоцитостимулирующую роль АКТГ, с 25 по 33 — иммуногенные свойства АКТГ данного вида животного (он более других участков различается у различных видов животных). Участок с 20 по 24 защищает АКТГ от действия экзопептидаз, играя роль стабилизатора. Такая множественность обладающих биологической активностью участков АКТГ обуславливает наличие нескольких биологических эффектов гормона и возможность связывания его с несколькими видами рецепторов.
По прошествии определенного периода времени молекула АКТГ может расщепиться на α-меланоцит-стимулирующий гормон и КЛИП, белок, роль которого ещё не изучена.
Биосинтез
АКТГ, как и некоторые другие гормоны (меланоцитостимулирующий гормон, липотропины и β-эндорфин), синтезируется из белка-предшественника проопиомеланокортина (пре-проопиомеланокортина). Удаление из пре-проопиомеланокортина в процессе трансляции сигнальной пептидной последовательности, приводит к образованию проопиомеланокортина, который, претерпев ряд посттрансляционных модификаций (фосфорилирование и гликозилирование), расщепляется эндопептидазами на различные полипептидные фрагменты с разной активностью.
Синтез АКТГ подчинён особому ритму, который, в свою очередь, подчинён ритму выделения кортиколиберина. Максимальная секреция АКТГ (а также либерина и глюкокортикоидов) наблюдается утром в 6-8 часов, а минимальная — между 18 и 23 часами.
Рецепторы АКТГ
Специфическим рецептором АКТГ считается MC2R — один из меланокортиновых рецепторов, расположенных в основном на клетках коры надпочечников и жировой ткани. Это семиспиральный рецептор, связанный c Gs-белком. Кроме того, АКТГ связывается с разной степенью аффинности с остальными меланокортиновыми рецепторами, которые расположены на многих типах клеток — клетках кожи, меланоцитах, клетках иммунной системы и др.
Физиологическая роль
Кортикотропин контролирует синтез и секрецию гормонов коры надпочечников (особенно их пучковой зоны). В основном кортикотропин влияет на синтез и секрецию глюкокортикоидов — кортизола, кортизона, кортикостерона. Попутно повышается синтез надпочечниками прогестерона, андрогенов и эстрогенов. Это может иметь как хронический, так и кратковременный характер. Относительно механизма стимуляции АКТГ синтеза кортикостероидов выдвигалось несколько теорий:
- Теория Хейнса (R. C. Haynes). Согласно Хейнсу, АКТГ повышает активность аденилатциклазы, катализирующей превращение АТФ в циклический 3’,5’- аденозинмонофосфат (3’,5’- АМФ), активирующий фосфорилазу. Фосфорилаза, в свою очередь, расщепляет гликоген надпочечников до глюкозо-1-фосфата, превращающегося далее в глюкозо-6-фосфат. Глюкозо-6-фосфат, обмениваясь через пентозный цикл, приводит к увеличению восстановленного никотинамидадениндинуклеотидфосфата (НАДФН2), являющегося необходимым кофактором при превращении холестерина в прегненолон и при гидроксилировании стероидных предшественников до конечных продуктов стероидогенеза.
- Теория МакКёрнса (K. W. McKerns). В целом сходна с предыдущей за исключением одного момента: она объясняет повышение концентрации НАДФН2 в надпочечниках не как результат усиления гликогенолиза, а как результат повышения активности глюкозо-6-фосфатдегидрогиназы.
- Теория Гаррена (L. D. Garren) с сотр. Согласно этой теории, АКТГ стимулирует аденилатциклазу в мембранах клеток и увеличивает поступление циклического 3’,5’- АМФ в цитоплазму, где 3’,5’- цАМФ взаимодействует с комплексом рецепторный белок — протеинкиназа и, вызывая его диссоциацию, активирует протеинкиназу. Протеинкиназа фосфорилирует рибосомы и стимулирует в них синтез специального белка, проходящий с использованием стабильной иРНК в качестве матрицы. Образовавшийся белок производит перенос свободного холестерина из жировых капель цитоплазмы в митохондрии, где находится белок P450scc, имеющий ферментативную функцию. Он ускоряет образование стероидов, началом которого является разложение холестерина, вследствие чего, из него образуется прегненолон, а затем и кортикостероиды (транскрипцию генов стероидогенных ферментов, к которым и принадлежит P450scc, способен стимулировать сам АКТГ при длительном действии).
На данный момент подтверждённой считается теория Гаррена.
В некоторой степени кортикотропин повышает также синтез и секрецию минералокортикоидов — дезоксикортикостерона и альдостерона. Однако кортикотропин не является основным регулятором синтеза и секреции альдостерона. Основной механизм регуляции синтеза и секреции альдостерона находится вне влияния оси гипоталамус — гипофиз — кора надпочечников — это ренин-ангиотензин-альдостероновая система.
Кортикотропин также в небольшой степени увеличивает синтез и секрецию катехоламинов мозговым веществом надпочечников. Однако кортикотропин не является основным регулятором синтеза катехоламинов в мозговом веществе надпочечников. Регуляция синтеза катехоламинов осуществляется в основном через симпатическую стимуляцию хромаффинной ткани надпочечников либо через реакцию хромаффинной ткани надпочечников на такие факторы, как её ишемия или гипогликемия.
Кортикотропин также повышает чувствительность периферических тканей к действию гормонов коры надпочечников (глюкокортикоидов и минералокортикоидов).
В больших концентрациях и при длительном воздействии кортикотропин вызывает увеличение размеров и массы надпочечников, особенно их коркового слоя, увеличение запасов холестерина, аскорбиновой и пантотеновой кислот в коре надпочечников, то есть функциональную гипертрофию коры надпочечников, сопровождающуюся увеличением общего содержания в них белка и ДНК. Объясняется это тем, что под влиянием АКТГ в надпочечниках повышается активность ДНК-полимеразы и тимидинкиназы — ферментов, участвующих в биосинтезе ДНК. Длительное введение АКТГ ведёт к увеличению активности 11-бета-гидроксилазы, сопровождающееся появлением в цитоплазме белкового активатора фермента. При повторных инъекциях АКТГ в организме человека также изменяются соотношения секретируемых кортикостероидов (гидрокортизона и кортикостерона) в сторону значительного увеличения секреции гидрокортизона.
Также АКТГ способен к меланоцитостимулирующей активности (он способен активировать переход тирозина в меланин) за счет последовательности 13-ти аминокислотных остатков N-концевого участка. Это объясняется схожестью последней с последовательностью аминокислот в α-меланоцитостимулирующем гормоне.
Большое число данных указывает на то, что АКТГ/МСГ-подобные пептиды способны ингибировать процессы воспаления.
АКТГ способен к взаимодействию с другими пептидными гормонами (пролактином, вазопрессином, TRH, VIP, опиоидными пептидами), а также с медиаторными системами моноаминов гипоталамуса. Установлено, что АКТГ и его фрагменты способны влиять на память, мотивацию, процессы обучения.
Помимо ключевой функции, заключающейся в регуляции секреции коры надпочечников, АКТГ регулирует многие процессы в различных клетках, например, в остеобластах, отвечающих за образование костной ткани. Влияние АКТГ на остеобласты было обнаружено в 2005 году. Исследования показали, что ответная реакция остеобластов на АКТГ включает в себя выработку фактора роста эндотелия сосудов, сигнального белка, стимулирующего формирование кровеносных сосудов. Такая ответная реакция в некоторых случаях может играть важную роль в выживании остеобластов.
Медицинское значение
В ряде случаев у пациентов определяют уровень АКТГ в крови. Нормальным считается уровень АКТГ 9-52 пг/мл. Повышенный уровень АКТГ наблюдается при болезни Аддисона (или первичной недостаточности) (причиной может быть поражение паренхимы надпочечников ,из-за чего нарушается синтез гормонов, что приводит к повышению уровня АКТГ в крови в результате гипокортицизма), болезни Кушинга, вызываемой опухолью гипофиза, ренолейкодистрофии, синдроме Нельсона и эктопических опухолях, продуцирующих АКТГ. Пониженный уровень АКТГ может наблюдаться при синдроме Кушинга, связанном с опухолями надпочечников, и при гипофизарной недостаточности.
При рецессивно-аутосомных мутациях рецептора АКТГ наблюдается семейный дефицит глюкокортикоидов.
Регуляция секреции
У человека синтез и секреция АКТГ в кровь регулируется гипоталамусом, выделяющим кортиколиберин — АКТГ-рилизинг-фактор. Синтезированные под действием АКТГ кортикостероиды выходят в кровь и воздействуют на гипоталамус и по механизму отрицательной обратной связи подавляют секрецию кортиколиберина. Кроме того, известно, что глюкокортикоиды могут также подавлять транскрипцию гена проопиомеланокортина и синтез полипептидной цепи.
Период полураспада АКТГ в крови человека составляет приблизительно десять минут.
Искусственный АКТГ
Искусственный АКТГ, состоящий из первых 24 аминокислот природного гормона, был впервые получен Клаусом Гофманном в Питтсбургском Университете. В синтетических формах АКТГ известен как Синактен или Кортрозин. Эти два вещества используются в Австралии и Великобритании для проведения АКТГ-тестов, показывающих эффективность работы надпочечников в стрессовых ситуациях.
Поначалу искусственный АКТГ использовали в качестве замены так называемого Актар геля для лечения эпилептических спазмов. Но из-за резко возросших цен лекарство потеряло популярность. Вскоре оно было также предложено для лечения аутоиммунных заболеваний и нефротических синдромов.
Открытие
Работая над диссертацией, Эвелин М. Андерсон, совместно с Джеймсом Бертрамом Коллипом и Дэвидом Томсоном Ландсборо, исследовала функцию АКТГ и объяснила её в статье, опубликованной в 1933 году.