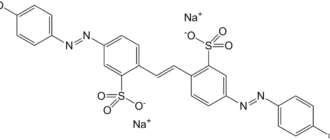
Конго красныйбифенила) — азокраситель, кислотно-основный индикатор.C.I.22120. C.I.Direct red 28. Синонимы — конгорот, Kongorot.
| Конго красный | |
|---|---|
| Общие | |
| Хим. формула | C32H22N6Na2O6S2 |
| Физические свойства | |
| Молярная масса | 696,665 г/моль |
| Термические свойства | Температура |
| • плавления | >360 °C |
| Классификация | |
| Рег. номер CAS | 573-58-0 |
| Рег. номер EINECS | 209-358-4 |
| InChI |
1S/C32H24N6O6S2.2Na/c33-31-25-7-3-1-5-23(25)29(45(39,40)41)17-27(31)37-35-21-13-9-19(10-14-21)20-11-15-22(16-12-20)36-38-28-18-30(46(42,43)44)24-6-2-4-8-26(24)32(28)34;;/h1-18H,33-34H2,(H,39,40,41)(H,42,43,44);;/q;2*+1/p-2/b37-35+,38-36+;;
IQFVPQOLBLOTPF-HKXUKFGYSA-L
|
| ChEBI | 34653 |
| ChemSpider | 10838 |
Получение
Конго красный получают взаимодействием диазотированного бензидина с нафтионовой кислотой.
Свойства
Внешний вид — красно-коричневые кристаллы. плохо растворим в холодной воде. Растворим в горячей воде и этаноле с образованием раствора красного цвета. В органических растворителях не растворяется. В спектре поглощения есть полоса с λmax = 505 нм. Раствор конго красного в нейтральной или слабокислой среде (рН 5,2) имеет красный цвет, в кислой среде (рН 3,0) — синий. В слабых кислотах (уксусной и др.) протонируется только одна азогруппа, в результате чего цвет может измениться в серо-фиолетовый вместо синего.
Применение
Конго красный используют в химическом анализе как индикатор, при броматометрическом определении гидразинсульфата. Индикатор применяется также для фотохимического определения нитратов по следующей методике: раствор конго красного в присутствии нитрата под влиянием УФ при pH 7-8 обесцвечивается; по уменьшению оптической плотности в течение определённого времени определяют содержание нитратов. Мешают — Br−, I−, NO2−; не мешают — Cl−, F−, SO42−, CH3COO−, PO43−, VO3−.
Также данный краситель находит применение в микроскопических исследованиях и используется, в виде спиртового, водного или аммиачного раствора для окрашивания клеточной оболочки грибов (самостоятельно, либо в сочетании с генциановым фиолетовым). Конго красный широко применяется в гистологии для выявления амилоида. Помимо этого «классического» применения, конго красный используется в десятках других процедур окрашивания в зоологии беспозвоночных, ботанических исследованиях, цитологии человека и животных.
Для крашения тканей не применяется из-за изменения цвета в растворах c разной кислотностью и несветопрочностью.