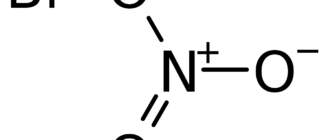Содержание
Нитрат бария, динитрáт бáрия) — неорганическое соединение, бариевая соль азотной кислоты. Химическая формула — Ba(NO3)2.
| Нитрат бария | |
|---|---|
| Общие | |
| Систематическое наименование |
Нитрат бария |
| Традиционные названия | Нитрат бария; бариевая селитра, азотнокислый барий, динитрат бария; нитрат бария(2+) |
| Хим. формула | Ba(NO3)2 |
| Рац. формула | Ba(NO3)2 |
| Физические свойства | |
| Состояние | кристаллическое |
| Молярная масса | 261,337 г/моль |
| Плотность | 3,24 г/см³ |
| Термические свойства | Температура |
| • плавления | 595 °C |
| Мол. теплоёмк. | 151,6 Дж/(моль·К) | Энтальпия |
| • образования | −978,6 кДж/моль |
| Химические свойства | Растворимость |
| • в воде | 4,95 г/100 мл (при 0 °C)
10,5 г/100 мл (при +25 °C) 34,4 (при 100 °C) |
| • в | спирте: нерастворим |
| Классификация | |
| Рег. номер CAS | 10022-31-8 |
| PubChem | 24798 |
| Рег. номер EINECS | 233-020-5 |
| SMILES |
[N+](=O)([O-])[O-].[N+](=O)([O-])[O-].[Ba+2]
|
| InChI |
1S/Ba.2NO3/c;2*2-1(3)4/q+2;2*-1
IWOUKMZUPDVPGQ-UHFFFAOYSA-N
|
| RTECS | CQ9625000 |
| ChemSpider | 23184 |
| Безопасность | |
| Предельная концентрация | 0,5 г/см3 |
| ЛД50 | (перорально, крысы) 355 мг/кг |
| Токсичность | умеренно-токсичен, ирритант, опасен для окружающей среды |
| NFPA 704 |
|
Распространение в природе
Нитрат бария встречается в природе в виде редкого минерала нитробаритa.
Физико-химические свойства
Нитрат бария представляет собой бесцветные кристаллы с кубической решеткой.
Термодинамические параметры
- Энтропия образования (298К): 96,4 Дж/(моль·К)
- Энтальпия плавления: 53,1 кДж/моль
Растворимость
- В воде
- растворим (9,2 г/100мл при +20 °C; 34,2 г/100мл при +100 °C);
- не растворим в спирте и концентрированной азотной кислоте.
С нитратом калия образует Ba(NO3)2•2KNO3.
Методы получения
- В лаборатории методом получения нитрата бария является взаимодействие гидроксида бария с азотной кислотой:
- При температуре выше 595 °C разлагается до нитрита:
-
- При температуре свыше 670 °C разлагается до оксида бария.
- При температуре свыше 670 °C разлагается до оксида бария.
Применение
- Для получения оксида и пероксида бария.
- Компонент эмалей и глазурей.
- В пиротехнике негигроскопичный нитрат бария широко используется для окрашивания пламени в зелёный цвет (большинство соединений других металлов, способных на это, мало пригодны из-за гигроскопичности).
Физиологическое значение
- Динитрат бария обладает умеренно-токсическим действием. ЛД50 для крыс при пероральном введении составляет 355 мг на 1 кг живого веса.
- Предельно допустимая концентрация азотнокислого бария в воздухе рабочих помещений составляет 0,5 г/см3 с обязательным контролем по ионам бария.
- Передозировка нитрата бария(2+) и других неорганических соединений этого щёлочноземельного металла в живых организмах — не безопасна.