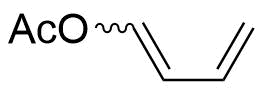
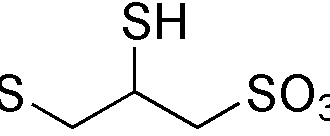
Морфолиновые олигонуклеотиды, или морфолиновые олигомеры — синтетические олигонуклеотиды, использующиеся в молекулярной биологии для изменения экспрессии генов. Основу молекулярной структуры морфолинового олигонуклеотида составляют метиленморфолиновые кольца и фосфородиамидатные связи. Морфолиновые олигонуклеотиды блокируют доступ других молекул к небольшим специфическим последовательностям за счёт комплементарного спаривания с соответствующей РНК. Морфолиновые олигонуклеотиды служат исследовательскими инструментами в обратной генетикe для нокдауна гена.
Нокдаун гена заключается в предотвращении синтеза клеткой соответствующего белка. Морфолиновые олигонуклеотиды также могут влиять на сплайсинг пре-мРНК. Нокдаун гена является мощным средством для изучения функции конкретного гена. Аналогичным образом, вырезание специфического экзона из транскрипта позволяет определить функции, выполняемые соответствующими аминокислотными остатками белка, а иногда приводит к полной инактивации белка. Морфолиновые олигонуклеотиды используются в изучении многих модельных организмов, в том числе мышей, данио-рерио, лягушек и морских ежей.
Разрабатываются пути применения морфолиновых олигонуклеотидов в медицине против патогенных организмов (бактерий и вирусов), а также для ослабления проявления генетических заболеваний.
Структура
Морфолиновые олигонуклеотиды — это синтетические молекулы, представляющие собой измененные нуклеиновые кислоты. Они, как правило, имеют длину 25 нуклеотидов и комплементарно связываются с соответствующими последовательностями РНК за счёт спаривания оснований. Морфолиновые олигонуклеотиды имеют обычные азотистые основания, которые вместо дезоксирибозы соединены с кольцами морфолина, а в связи отдельных нуклеотидов участвуют не фосфатные, а фосфородиамидатные группы. Замена отрицательно заряженных фосфатных групп незаряженной фосфородиамидатной группой устраняет ионизацию при физиологических значениях рН, так что в живых клетках эти молекулы не заряжены. Вся молекула морфолинового олигонуклеотида состоит из таких изменённых нуклеотидов.
Функции
Нормальная экспрессия гена
Трансляция заблокирована морфолиновым олигонуклеотидом
Сплайсинг заблокирован морфолиновым олигонуклеотидом
Морфолиновые олигонуклеотиды не вызывают деградации своей РНК-мишени, в отличие от многих антисмысловых молекул (например, малых интерферирующих РНК и фосфоротиоатов). Вместо этого они выступают в роли «пространственных блокаторов», связываясь с последовательностью-мишенью и физически не давая другим молекулам связаться с этой РНК. Морфолиновые олигонуклеотиды часто используются для изучения роли специфических мРНК в развивающемся зародыше. Эмбриологи инъецируют их в яйца или зародыши данио-рерио, шпорцевой лягушки, морских ежей и рыбы Fundulus heteroclitus* или доставляют эти молекулы путём электропорации в зародыши курицы на более поздних стадиях развития; обработанные таким образом зародыши называют морфантами. При наличии в цитозоле правильных систем доставки морфолиновых олигонуклеотидов могут быть эффективными и в культурах клеток.
Блокирование трансляции
Связываясь с 5′-нетранслируемой областью мРНК, морфолиновые олигонуклеотиды могут мешать рибосоме в комплексе с эукариотическими факторами инициации трансляции двигаться от кэпа к старт-кодону. Это предотвращает трансляцию кодирующей области транскрипта-мишени (нокдаун гена). Такой приём очень удобен, когда исследователь хочет определить функцию конкретного белка; по эффектам, оказываемым нокдауном гена на клетку или организм, судят о функции белка. Некоторые морфолиновые олигонуклеотиды блокируют экспрессию столь эффективно, что после деградации белка, синтезированного до введения олигонуклеотидов, этот белок становится неопределимым при помощи вестерн-блоттинга.
Изменение сплайсинга пре-мРНК
Морфолиновые олигонуклеотиды могут вмешиваться в процессинг пре-мРНК следующими способами:
- предотвращая связывание направляющих сплайсинг малых ядерных рибонуклеопротеинов (snRNP) со своими мишенями на границах интронов в пре-мРНК;
- блокируя остаток аденина, осуществляет нуклеофильную атаку в ходе сплайсинга и образует структуру лассо;
- мешая связыванию регуляторных белков сплайсинга, таких как сайленсеры и энхансеры сплайсинга.
Предотвращение связывания рибонуклеопротеинов U1 (в сайте-доноре) или U2/U5 (в полипиримидиновом тракте или сайте-акцепторе) может привести к модифицированному сплайсингу, при котором из зрелой мРНК исключаются экзоны. Воздействие на другие сайты сплайсинга приводит к включению интронов в зрелую мРНК, в то время как активация скрытых сайтов сплайсинга может приводит и к включениям, и к исключениям. Морфолиновые олигонуклеотиды могут также блокировать мишени snRNP U11/U12. Изменения в сплайсинге удобно отслеживать при помощи ПЦР с обратной транскрипцией (RT-PCR) и электрофореза (при электрофорезе продуктов RT-PCR наблюдается смещение полос в геле).
Другие применения
Морфолиновые олигонуклеотиды использовались для блокировки активности микроРНК, а также их созревания. Морфолиновые олигонуклеотиды, меченные флуоресцеином, в сочетании с антителами, специфичными к флуоресцеину, могут использоваться в качестве проб in situ-гибридизации с микроРНК. Кроме того, они могут блокировать активность рибозимов, а также функционирование snRNP U2 и U12. Морфолиновые олигонуклеотиды, нацеленные на «оголённые» последовательности мРНК в пределах кодирующей области, могут вызывать сдвиг рамки считывания при трансляции. Они также могут блокировать редактирование РНК. Эффективность морфолиновых олигонуклеотидов по отношению ко многим мишеням делает их универсальным средством для подавления взаимодействия белков или нуклеиновых кислот с мРНК.
Специфичность, стабильность и не-антисмысловые эффекты
Морфолиновые олигонуклеотиды стали стандартным инструментом для нокдауна генов в эмбриональных системах животных, в которых экспрессируется больше генов, чем во взрослых клетках. После инъекции морфолинового олигонуклеотида в зародыши лягушки или рыбы на стадии одной или нескольких клеток наибольший эффект проявляется к пятому дню, когда большая часть органогенеза и дифференцировки клеток и тканей уже позади; наблюдаемые фенотипы соответствуют нокауту определённого гена. Контрольные нуклеотиды, не нацеленные на какие-либо последовательности, как правило, не вызывают изменений в фенотипе зародыша, подтверждая, что морфолиновые олигонуклеотиды действуют специфично к последовательностям и, как правило, не имеют не-антисмысловых эффектов. Дозу, необходимую для нокдауна гена, можно сократить, одновременно вводя несколько морфолиновых олигонуклеотидов, нацеленных на одну и ту же мРНК; этот приём позволяет сократить или вовсе исключить зависимые от дозы взаимодействия олигонуклеотидов с РНК, не являющимися непосредственными мишенями.
В экспериментах по «спасению» мРНК у зародышей часто удавалось вернуть фенотип дикого типа. В ходе этих экспериментов морфолиновый олигонуклеотид вводится в клетку вместе с мРНК, кодирующей тот белок, на нокдаун которого этот олигонуклеотид и направлен. Однако вводимая мРНК имеет изменённую 5′-нетранслируемую область, а потому не имеет последовательности-мишени для морфолинового олигонуклеотида, но её кодирующая область сохранена и с неё синтезируется интересующий белок. Трансляция с мРНК-«спасателя» восстанавливает образование белка, остановленное морфолиновым олигонуклеотидом. Спасательная мРНК не вызывает фенотипических отклонений, так как не действует на экспрессию генов, не являющихся мишенью введенного олигонуклеотида, поэтому возврат к фенотипу дикого типа служит ещё одним доказательством специфичности морфолиновых олигонуклеотидов по отношению к последовательности.
Из-за совершенно неестественного химического строения морфолиновые олигонуклеотиды не распознаются клеточными белками. Нуклеазы их не разрушают, поэтому они не разрушаются ни в клетках, ни в плазме крови. Морфолиновые олигонуклеотиды не активируют Toll-подобные рецепторы, а потому не запускают врождённый иммунный ответ, выражающийся, в частности, в образовании интерферона или в NF-κB-опосредованном воспалении.
До 18 % морфолиновых олигонуклеотидов вызывают не связанные с исходными мишенями фенотипы, в частности, смерть клеток центральной нервной системы и сомитов у зародышей данио-рерио. Было показано, что большая часть этих эффектов связана с активацией p53-опосредованного апоптоза; их можно подавить, одновременно вводя экспериментальный морфолиновый олигонуклеотид и его анти-p53-аналог. Более того, вызванную морфолиновым олигонуклеотидом активацию p53-опосредованного апоптоза удалось повторить с использованием других антисмысловых структур, что говорит в пользу того, что p53-опосредованный апоптоз может быть вызван утратой белка-мишени и не зависит от типа олигонуклеотида, используемого для нокдауна.
Морфолиновые олигонуклеотиды следует использовать с осторожностью из-за их потенциальных эффектов вне белка-мишени. Для проверки того, является ли наблюдаемый фенотип морфанта результатом нокдауна задуманного гена или же он вызван взаимодействием с РНК, не являющейся непосредственной мишенью введенного олигонуклеотида, можно провести второй эксперимент. Этот эксперимент заключается в повторении фенотипа (фенокопировании) морфанта с использованием другого морфолинового олигонуклеотида, нацеленного на ту же мишень, но не перекрывающегося с первым олигонуклеотидом.
Доставка
Для того, чтобы морфолиновый олигонуклеотид мог подействовать, он должен попасть в цитозоль клетки и преодолеть клеточную мембрану. После попадания в цитозоль он начинает свободно диффундировать между цитозолем и ядром, как было показано в экспериментах, при которых введение морфолинового нуклеотида в цитозоль клетки изменяло сплайсинг в ядре. Для доставки морфолинового олигонуклеотида в зародыши, клетки культуры или клетки взрослых животных используются различные методы.
Для доставки в зародыши, как правило, используют микроинъекции, причём введение олигонуклеотидов обычно осуществляют на стадии одной или нескольких клеток. Альтернативный метод для доставки морфолиновых олигонуклеотидов в эмбрионы — электропорация, которая позволяет доставить их в ткани на более поздних стадиях развития зародыша.
Наиболее распространённые методы для доставки морфолиновых олигонуклеотидов в клетки культуры — использование эндопортерного пептида (англ. Endo-Porter peptide), который вызывает высвобождение морфолиновых олигонуклеотидов из эндосом; система специальной доставки (англ. Special Delivery system), использующая гетеродуплекс ДНК с морфолиновым олигонуклеотидом и этоксилированный полиэтиленимин в качестве реагента доставки (больше коммерчески недоступна); электропорация; метод соскоба-загрузки (англ. scrape loading). В 2015 году была описана транс-активирующая амфипатическая система доставки, основанная на ДНК, которая предназначена для удобной доставки незаряженных нуклеиновых кислот, имеющих поли(А)-хвост, таких как пептидо-нуклеиновые кислоты и морфолиновые олигонуклеотиды.
Доставка морфолиновых олигонуклеотидов в ткани взрослых животных затруднительна, хотя разработано несколько систем, позволяющих доставить в ткани немодифицированные морфолиновые олигонуклеотиды (в частности, в от природы слабые мышечные клетки при мышечной дистрофии Дюшена или в клетки сосудистого эндотелия, подвергающиеся стрессу при ангиопластии). Хотя морфолиновые олигонуклеотиды эффективно проходят через межклеточные промежутки в тканях, доставка их в клетки сложна. Системная доставка в клетки многих типов может быть осуществлена при помощи морфолиновых олигонуклеотидов, ковалентно связанных с проникающими в клетки пептидами (англ. Cell-penetrating peptide), и, в то время как токсичный эффект оказывают средние дозы связанных пептидов, в условиях in vivo удалось добиться эффективной доставки морфолиновых олигонуклеотидов при дозах пептидов ниже токсичных. Октагуанидиновый дендример, прикреплённый к концу морфолинового олигонуклеотида (т. н. Vivo-Morpholino), обеспечивает его доставку из крови в цитозоль при систематическом введении во взрослого животного.
Медицинское значение
Морфолиновые олигонуклеотиды, способные к эффективной доставке (такие как связанные с пептидами морфолиновые олигонуклеотиды и Vivo-Morpholino), могут быть перспективными средствами для лечения вирусных и генетических заболеваний. Например, Sarepta Therapeutics Inc. уже разрабатывает морфолиновые олигонуклеотиды — потенциальные лекарства под названием NeuGene. В настоящее время проходят клинические испытания морфолиновые олигонуклеотиды, которые могут использоваться для лечении миодистрофии Дюшенна у человека.