Ацетальдоксим — органическое вещество класса оксимов, производное ацетальдегида и гидроксиламина.
| Ацетальдоксим | |
|---|---|
| Общие | |
| Традиционные названия | оксим ацетальдегида |
| Хим. формула | C2H5NO |
| Физические свойства | |
| Плотность | 0,969 г/см³ |
| Термические свойства | Температура |
| • плавления | 47 °C (смесь изомеров) |
| • кипения | 114–115 °C (смесь изомеров) °C |
| • вспышки | 40 °C |
| Оптические свойства | |
| Показатель преломления | 1,426 |
| Классификация | |
| Рег. номер CAS | 107-29-9 |
| PubChem | 24890491 |
| Рег. номер EINECS | 203-479-6 |
| SMILES |
CC=NO
|
| InChI |
1/C2H5NO/c1-2-3-4/h2,4H,1H3
FZENGILVLUJGJX-UHFFFAOYSA-N
|
| ChEBI | 28465 |
| ChemSpider | 7575 |
| Безопасность | |
| Краткие характер. опасности (H) |
H226, H302, H319, H332
|
| Меры предостор. (P) |
P305+P351+P338
|
| Сигнальное слово | Осторожно |
| Пиктограммы СГС |   |
Получение
Препаративным способом получения ацетальдоксима является реакция свежеперегнанного ацетальдегида с гидроксиламином в присутствии гидроксида натрия.

Строение и физические свойства
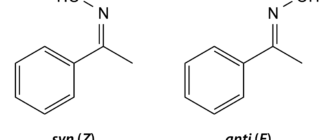
Ацетальдоксим является несимметричным оксимом, поэтому существует в виде смеси (E)/(Z)-изомеров, которые также иногда называют син/анти-изомерами. В литературе сообщается, что в чистом ацетальдоксиме присутствует около 40 % (Е)-изомера, а в кислом растворе — 46 % (Е)-изомера. Чистый (Z)-изомер можно получить медленной кристаллизацией из смеси изомеров. Установить конфигурацию ацетальдоксима можно при помощи ЯМР-спектроскопии.

(Z)-изомер (слева) и (E)-изомер (справа)
Ацетальдоксим растворим во многих органических растворителях, в том числе хлороформе, тетрагидрофуране, бензоле, диэтиловом эфире и 1,2-дихлорэтане.
Химические свойства
В органическом синтезе ацетальдоксим используется в качестве эквивалента ацетальдегида, для ацетилирования ароматических соединений через промежуточное получение соответствующих солей диазония, для синтеза других альдоксимов путём алкилирования по метильной группе. При нагревании в присутствии ацетата никеля или силикагеля ацетальдоксим перегруппировывается в ацетамид. Также он участвует в реакциях диполярного циклоприсоединения и служит источником N-оксида ацетонитрила.