Содержание
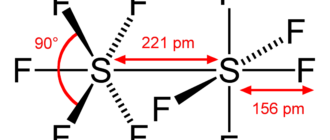
Тетрафторид серы) — неорганическое соединение с формулой SF4, бесцветный газ, реагирует с водой.
| Тетрафторид серы | |
|---|---|
| Общие | |
| Систематическое наименование |
Тетрафторид серы |
| Традиционные названия | Фтористая сера |
| Хим. формула | SF4 |
| Физические свойства | |
| Состояние | бесцветный газ |
| Молярная масса | 108,06 г/моль |
| Плотность | 1,9191-3 г/см³ |
| Энергия ионизации | 12,63 ± 0,01 эВ |
| Термические свойства | Температура |
| • плавления | -124; -122; -121,0 °C |
| • кипения | -40; -38; -37 °C | Критическая точка | 90,1 °C |
| Мол. теплоёмк. | 70,98 Дж/(моль·К) | Энтальпия |
| • образования | -770 кДж/моль |
| Давление пара | 10,5 ± 0,1 атм |
| Классификация | |
| Рег. номер CAS | 7783-60-0 |
| PubChem | 24555 |
| Рег. номер EINECS | 232-013-4 |
| SMILES |
FS(F)(F)F
|
| InChI |
1S/F4S/c1-5(2,3)4
QHMQWEPBXSHHLH-UHFFFAOYSA-N
|
| RTECS | WT4800000 |
| ChEBI | 30495 |
| Номер ООН | 2418 |
| ChemSpider | 22961 |
| Безопасность | |
| NFPA 704 |
|
Получение
- Действие хлора под давлением на смесь серы и фторида натрия:
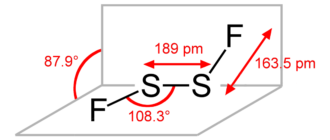
- Разложение дифторида дисеры:
Применение
С помощью тетрафторида серы производят фторирование различных соединений: он способен замещать фтором группу OH в спиртах, кислород в группе CO альдегидов, кислот, кетонов и даже замещать атом кислорода и группу OH в карбоксильной группе тремя атомами фтора:284 [1].
Безопасность
Тетрафторид серы очень ядовит. Реагируя со влагой воздуха, он образует пары фтористого водорода, глубоко поражающего живые ткани, а также сернистый газ. SF4 даже в малых количествах сильно раздражает глаза и слизистые мембраны, оказывает отравляющее действие при вдыхании. Поражает лёгкие, верхнюю часть пищеварительного тракта, кожу. [2]