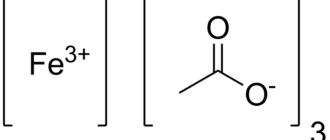
Оксалат железа(II) — неорганическое соединение, соль металла железа и щавелевой кислоты с формулой FeC2O4, желтовато-белые кристаллы, слабо растворяется в воде, образует кристаллогидрат.
| Оксалат железа(II) | |
|---|---|
| Общие | |
| Систематическое наименование |
Оксалат железа(II) |
| Традиционные названия | щавелевокислое железо |
| Хим. формула | FeC2O4 |
| Физические свойства | |
| Состояние | желтовато-белые кристаллы |
| Молярная масса | 143,86 г/моль |
| Плотность | гидрат 2,28 г/см³ |
| Химические свойства | Растворимость |
| • в воде | 0,0725 г/100 мл |
| Классификация | |
| Рег. номер CAS | 516-03-0 |
| PubChem | 10589 |
| Рег. номер EINECS | 208-217-4 |
| SMILES |
C(=O)(C(=O)[O-])[O-].[Fe+2]
|
| InChI |
1S/C2H2O4.Fe/c3-1(4)2(5)6;/h(H,3,4)(H,5,6);/q;+2/p-2
OWZIYWAUNZMLRT-UHFFFAOYSA-L
|
| ChemSpider | 10144 |
Получение
- Действие оксалатами щелочных металлов на растворимые соли железа(II):
-
- Действие щавелевой кислоты на железо
- Fe + С2H2O4 = FeC2O4 + H2
Физические свойства
Оксалат железа(II) образует желтовато-белые кристаллы.
Образует кристаллогидрат состава FeC2O4•2H2O.
Слабо растворяется в воде.
Химические свойства
- Температурное разложение оксалата железа (II) известно получением при нем пирофорного железа, самовоспламеняющегося на воздухе. В среде углекислого газа пирофорное железо медленно восстанавливает CO2 до CO. Если перевернуть пробирку сразу после нагревания, то пирофорное железо будет сгорать, покинув среду CO2.
- Гидрат обезвоживается при 200°С.
- При смешении с раствором оксалата аммония или щелочного металла в подкисленной среде образует комплексную соль: