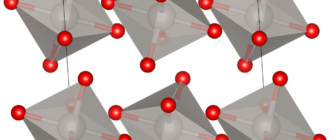
Метагидроксид марганца — неорганическое соединение, оксогидроксид металла марганца с формулой MnO(OH), буро-чёрные кристаллы, не растворимые в воде.
| Метагидроксид марганца | |
|---|---|
| Общие | |
| Систематическое наименование |
Метагидроксид марганца |
| Традиционные названия | гидроокись марганца (III) |
| Хим. формула | MnO(OH) |
| Физические свойства | |
| Состояние | буро-чёрные кристаллы |
| Молярная масса | 87,9439 г/моль |
| Плотность | 4,2; 4,14; 4,335 г/см³ |
| Твёрдость | 4 (по шкале Мооса) |
| Термические свойства | |
| Мол. теплоёмк. | 62,8 Дж/(моль·К) |
| Классификация | |
| PubChem | 5359598 |
| SMILES |
O[Mn]=O
|
| InChI |
1S/Mn.H2O.O/h;1H2;/q+1;;/p-1
RMLMSMONVBVHNA-UHFFFAOYSA-M
|
| ChemSpider | 4514332 |
Получение
- В природе встречается минерал манганит — MnO(OH) с различными примесями.
- Растворение оксида марганца(IV) в концентрированном холодном едком натре:
Физические свойства
Метагидроксид марганца образует парамагнитные буро-чёрные кристаллы моноклинной сингонии, пространственная группа P 21/b, параметры ячейки a = 0,527 нм, b = 0,524 нм, c = 0,527 нм, β = 114,50°, Z = 4.
Есть упоминание о существовании другой модификации ромбической сингонии, пространственная группа P bnm, параметры ячейки a = 0,453 нм, b = 0,927 нм, c = 0,287 нм, Z = 4.
Не растворяется в воде, р ПР = 36,0.
Химические свойства
- Разлагается при нагревании в вакууме:
- Реагирует с кислотами:
- Растворяется в растворе, содержащем щавелевую кислоту и оксалат калия, с образованием комплексного соединения:
- Реагирует с перегретыми растворами щелочей (под давлением):
- Окисляет концентрированную горячую соляную кислоту:
- Окисляется кислородом воздуха при нагревании:
- В присутствии влаги медленно окисляется при комнатной температуре:
- Восстанавливается водородом: