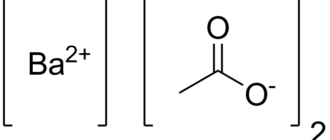
Карбонат бария — химическое соединение, бариевая соль угольной кислоты. Химическая формула BaCO3. В природе встречается в виде минерала витерита.
| Карбонат бария | |
|---|---|
| Общие | |
| Систематическое наименование |
Карбонат бария |
| Традиционные названия | Карбонат бария; углекислый барий, витерит |
| Хим. формула | BaCO3 |
| Рац. формула | BaCO3 |
| Физические свойства | |
| Молярная масса | 197,34 г/моль |
| Плотность | 4,286 г/см³ |
| Термические свойства | Температура |
| • разложения | >1400 °C | Энтальпия |
| • образования | −1211 кДж/моль |
| Химические свойства | Растворимость |
| • в воде | (при 20 °C) 0,0024 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,60 |
| Классификация | |
| Рег. номер CAS | 513-77-9 |
| PubChem | 10563 |
| Рег. номер EINECS | 208-167-3 |
| SMILES |
[Ba+2].[O-]C([O-])=O
|
| InChI |
1S/CH2O3.Ba/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2
AYJRCSIUFZENHW-UHFFFAOYSA-L
|
| RTECS | CQ8600000 |
| Номер ООН | 1564 |
| ChemSpider | 10121 |
| Безопасность | |
| ЛД50 | 418 мг/кг (крысы, перорально) |
| Токсичность | ирритант, среднетоксичен |
| NFPA 704 |
|
Обладает умеренно-токсическим действием. Может использоваться в качестве компонента отравленных приманок.
Физические свойства
Углекислый барий (BaCO3) представляет собой бесцветные кристаллы. До 810 °C устойчива α-модификация с ромбической решёткой; в интервале 810—960 °C — β-модификация с гексагональной решёткой; свыше 960 °C — γ-модификация с кубической решёткой.
Tпл 1555 °C (в атмосфере CO2 под давлением 45 МПа). Плохо растворим в воде (ПР = 8⋅10−9 при 20 °C). Растворимость повышается в присутствии ионов аммония или угольной кислоты. Образует твердые растворы с CaCO3 и SrCO3, BaO. C BaCl2 и BaTiO3 дает эвтектические смеси.
Получение
В промышленности, обычно, карбонат бария получают из минерального сырья; кроме того возможны следующие химические способы его получения:
- Взаимодействие BaS с CO2 или Na2CO3:
- Обменная реакция растворимых солей бария или гидроксида бария с растворами карбонатов:
Химические свойства
- Реагирует с разбавленной соляной, азотной и уксусной кислотами:
- При нагревании свыше 1400 °C разлагается:
- В отличие от карбоната кальция не образует гидрокарбонат под действием CO2 в водной среде.
Применение
Применяется в компонентах смесей для производства катодов различных электровакуумных приборов. Например, смесь «Radio Mix No. 3» от фирмы «J. T. Baker Chemical Co.» состоит на 57,3 % из карбоната бария, который при нагревании в вакууме разлагается до оксида бария.
Компонент шихты в производстве оптического стекла, эмалей, глазури и керамических изделий.
Карбонат бария используется как химический стандарт для калибровки калориметров по температуре и теплоемкости.
В России «барий углекислый технический» выпускается в соответствии с ГОСТ 2149-75.
Биологическая роль
Карбонат бария BaCO3 является умеренно-ядовитым веществом для крыс — ЛД50 составляет 418 мг/кг (при пероральном введении). Однако передозировка ионов бария Ba2+ в живых организмах явно небезопасна.